Cho 11,2 lít hỗn hợp khí mêtan và axetilen đi qua 50 ml dung dịch brôm 2M đến khi phản ứng xảy ra hoàn toàn. Tìm tỉ lệ % theo thể tích mỗi khí trong hỗn hợp ban đầu. Các chất khí đo ở đktc

Những câu hỏi liên quan
Hỗn hợp X gồm: etan , etilen , axetilen và hiđro , trong đó thể tích etan bằng 1/6 thể tích của hiđrocacbon. Nung nóng 2240 ml hỗn hợp X với xúc tác Ni thì được 1344 ml hỗn hợp khí Y. Cho hỗn hợp Y đi châmk qua dung dịch nước Brôm dư thu được một khí Z thoát rakhỏi dung dịch , lượng Brôm đã phản ứng là 6,4 gam. Tính phần trăm thể tích mỗi khí trong hỗn hợp X. Biết các thể tích khí đều được đo ở đktc và các phản ứng sảy ra hoàn toàn.
Đọc tiếp
Hỗn hợp X gồm: etan , etilen , axetilen và hiđro , trong đó thể tích etan bằng 1/6 thể tích của hiđrocacbon. Nung nóng 2240 ml hỗn hợp X với xúc tác Ni thì được 1344 ml hỗn hợp khí Y. Cho hỗn hợp Y đi châmk qua dung dịch nước Brôm dư thu được một khí Z thoát rakhỏi dung dịch , lượng Brôm đã phản ứng là 6,4 gam. Tính phần trăm thể tích mỗi khí trong hỗn hợp X. Biết các thể tích khí đều được đo ở đktc và các phản ứng sảy ra hoàn toàn.
Hỗn hợp A gồm
CH
4
,
C
2
H
2
và một hiđrocacbon X có công thức
C
n
H
2
n
+
2
.Cho 0,8...
Đọc tiếp
Hỗn hợp A gồm CH 4 , C 2 H 2 và một hiđrocacbon X có công thức C n H 2 n + 2 .Cho 0,896 lít hỗn hợp A đi qua dung dịch brom dư để phản ứng xảy ra hoàn toàn, thấy thoát ra 0,448 lít hỗn hợp hai khí. Biết rằng tỉ lệ số mol của CH 4 và C n H 2 n + 2 trong hỗn hợp là 1 : 1, khi đốt cháy 0,896 lít A thu được 3,08 gam khí CO 2 (thể tích khí đo ở đktc). Tính thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp A.
Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%
Đúng 0
Bình luận (0)
Cho 11,2 lít (đktc) hỗn hợp gồm axetilen và metan đi qua dung dịch Brom dư, sau khi phản ứng hoàn toàn thấy thoát ra 4,48 lít khí (đktc). Viết PTPU và tính % thể tích axetilen trong hỗn hợp
Giúp mình với, cảm ơn nhiềunhiều
Cho 6,72 lít hỗn hợp A gồm etilen và axetilen có tỉ khối so với hiđro là 40/3 lội qua 1,5 lít dung dịch Br2 0,2M. Sau khi phản ứng xong, thấy dung dịch brom mất màu hoàn toàn; khối lượng dung dịch brom tăng 5,88 gam và có 1,792 lít hỗn hợp khí B thoát ra khỏi bình. Các thể tích khí đều đo ở đktc. a. Tính khối lượng mỗi sản phẩm thu được. b. Tính thành phần % theo thể tích mỗi khí trong hỗn hợp B.
Đọc tiếp
Cho 6,72 lít hỗn hợp A gồm etilen và axetilen có tỉ khối so với hiđro là 40/3 lội qua 1,5 lít dung dịch Br2 0,2M. Sau khi phản ứng xong, thấy dung dịch brom mất màu hoàn toàn; khối lượng dung dịch brom tăng 5,88 gam và có 1,792 lít hỗn hợp khí B thoát ra khỏi bình. Các thể tích khí đều đo ở đktc.
a. Tính khối lượng mỗi sản phẩm thu được.
b. Tính thành phần % theo thể tích mỗi khí trong hỗn hợp B.
Cho 13,44 lít hỗn hợp khí (đktc) gồm Metan và Axetilen tác dụng hoàn toàn với 200 ml dung dịch Brom 1M.
a./ Tính % thể tích mỗi khỉ có trong hỗn hợp
b/ Nếu dân 6,72 lít hỗn hợp khí trên đi qua bình đựng dung dịch brôm, thì khối lượng của bình sẽ tăng lên bao nhiêu gam?
nhh = 13.44/22.4 = 0.6 (mol)
nBr2 = 0.2 (mol)
C2H2 + 2Br2 => C2H2Br4
0.1______0.2
nCH4 = 0.6 - 0.1 = 0.5 (mol)
%CH4 = 0.5/0.6 * 100% = 83.33%
%C2H2 = 16.67%
13.44 (l) => 0.1 (mol) C2H2
6.72 (l) => x(mol) C2H2
=> x = 0.05
m tăng = mC2H2 = 0.05*26= 1.3 (g)
Đúng 1
Bình luận (0)
Câu 3: Cho 3,36 lít hỗn hợp metan và axetilen sục vào dung dịch brom dư thấy có 2,4g brom tham gia phản ứng. a) Viết phương trình phản ứng hóa học xảy ra. b) Tính thể tích các khí trong hỗn hợp ban đầu biết các khí đo ở đktc. c) Tính % thể tích mỗi khí có trong hỗn hợp ban đầu?
\(n_{hh}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_{Br_2}=\dfrac{2,4}{160}=0,015mol\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,0075 0,015 ( mol )
\(V_{C_2H_2}=0,0075.22,4=0,168l\)
\(V_{CH_4}=3,36-0,168=3,192l\)
\(\%V_{C_2H_2}=\dfrac{0,168}{3,36}.100=5\%\)
\(\%V_{CH_4}=100\%-5\%=95\%\)
Đúng 4
Bình luận (0)
Cho 30,7 gam hỗn hợp gồm kẽm và sắt tác dụng hoàn toàn với dung dịch HCl 2M, sau phản ứng thu được 11,2 lít khí ở đktc. a) Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu b) Tính thể tích dung dịch HCl đã phản ứng
a,\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: x x
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}65x+56y=30,7\\x+y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Zn}=\dfrac{0,3.65.100\%}{30,7}=63,52\%;\%m_{Fe}=100\%-63,52\%=36,48\%\)
b,
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,3 0,6
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,4
nHCl = 0,6+0,4 = 1 (mol)
\(V_{ddHCl}=\dfrac{1}{2}=0,5\left(l\right)=500\left(ml\right)\)
Đúng 2
Bình luận (0)
Dẫn 11,2 lít khí (đktc) hỗn hợp A gồm metan và axetilen đi qua dung dịch brom, thấy có 48 gam brom tham gia phản ứng. a. Tính thành phần % thể tích trong hỗn hợp ban đầu b. Tính thể tích khí thoát ra ngoài
a, \(n_{Br_2}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
_____0,15____0,3 (mol)
\(\Rightarrow\%V_{C_2H_2}=\dfrac{0,15.22,4}{11,2}.100\%=30\%\)
\(\Rightarrow\%V_{CH_4}=100-30=70\%\)
b, - Khí thoát ra ngoài là CH4.
\(V_{CH_4}=11,2.70\%=7,84\left(l\right)\)
Đúng 1
Bình luận (1)
Một hỗn hợp A gồm etan (C2H6), etilen, axetilen, hiđro. Tỉ khối của hỗn hợp A so với CO2 là 0,4. Cho 11,2 lít hỗn hợp A đi qua dung dịch Br2 dư thấy khối lượng bình Br2 tăng thêm m gam. Hỗn hợp khí B thoát ra khỏi bình Br2 có thể tích 6,72 lít, trong đó khí có khối lượng phân tử nhỏ hơn chiếm 11,765% về khối lượng. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. a. Viết các phương trình hóa học xảy ra. b. Tính phần trăm thể tích các khí trong B. c. Tính m gam...
Đọc tiếp
Một hỗn hợp A gồm etan (C2H6), etilen, axetilen, hiđro. Tỉ khối của hỗn hợp A so với CO2 là 0,4. Cho 11,2 lít hỗn hợp A đi qua dung dịch Br2 dư thấy khối lượng bình Br2 tăng thêm m gam. Hỗn hợp khí B thoát ra khỏi bình Br2 có thể tích 6,72 lít, trong đó khí có khối lượng phân tử nhỏ hơn chiếm 11,765% về khối lượng. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn.
a. Viết các phương trình hóa học xảy ra.
b. Tính phần trăm thể tích các khí trong B.
c. Tính m gam.
a. Phương trình phản ứng :
C2H2 + 2Br2 → C2H2Br4 (1)
C2H4 + Br2 → C2H4Br2 (2)
b. Hỗn hợp khí B gồm có H2, C2H6. Gọi x, y ( mol ) lần lượt là số mol của H2 và C2H6 có trong 6,72 lít hỗn hợp B.
nB = x + y = 6,72 : 22,4 = 0,3 mol (I)
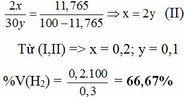
% V(C2H6) = 100% – 66,67% = 33,33%
c. nA = 11,2 : 22,4 = 0,5 mol , M A = 0,4 . 44 = 17,6 g/ mol
mA = 0,5 . 17,6 = 8,8 gam
mB = 0,2 . 2 + 0,1 . 30 = 3,4 gam
Vậy khối lượng bình Br2 tăng: m = mA – mB = 8,8 – 3,4 = 5,4 gam.
Đúng 0
Bình luận (0)




















